au sommaire
Même si cela ne nous saute pas aux yeuxyeux, certaines propriétés de l'eau sont étonnantes. Au contraire de tous les autres corps, elle ne se contracte pas en refroidissant, ce qui ferait couler les glaçons au fond des verresverres. Autre exemple : plus elle est froide, mieux elle dissout les gaz, une caractéristique qui permet aux poissonspoissons de respirer. Certaines de ces bizarreries ont été expliquées, par la taille et la topologie des molécules d'eau entre autres. Mais beaucoup de mystères restent à élucider.
En incluant des phénomènes quantiques à leurs modèles, des chercheurs britanniques du Laboratoire national de physique (NPL) ont voulu rendre la simulation du comportement des matériaux en général, et de l'eau en particulier, plus intuitive et plus proche de la réalité. C'est ainsi qu'avec la collaboration de l'Institut national de mesure, d'IBMIBM et de l'université d'Édimbourg, ils ont pu déterminer la structure moléculaire de la surface de l'eau à l'état liquideétat liquide.
L'interface liquide-vapeur à la surface de l'eau est l'un des environnements hétérogènes à la fois le plus commun et le plus mystérieux. Les mesures expérimentales de sa structure moléculaire sont délicates à réaliser et les modèles actuels ne s'entendent pas sur les résultats. Pourtant, comprendre la structure moléculaire de la surface de l'eau pourrait permettre de mieux comprendre les interactions qui sous-tendent de nombreux processus biologiques.
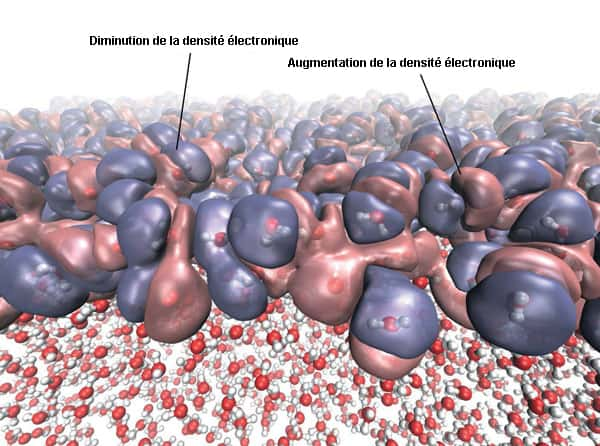
Les orientations moléculaires diverses à l’interface liquide-vapeur de l'eau créent une densité électronique hétérogène. © National Physical Laboratory
Le comportement des électrons est l'une des clés
Le modèle quantique utilisé par les chercheurs du NPL est basé sur une particule chargée fictive, nommée oscillateur de Drude. Dans le cas d'une molécule d'eau, cette particule est attachée à l'atome d'oxygène par le biais d'un ressort harmonique, mimant la façon dont les électrons d'une véritable molécule d'eau oscillent et réagissent à leur environnement. Des informations auxquelles les modèles classiques ne donnent généralement pas accès et qui, surtout, donnent une idée précise des propriétés moléculaires de l'eau liquide.
C'est la première fois que le modèle de l'oscillateur de Drude est appliqué à une interface liquide-vapeur. Les résultats des chercheurs britanniques montrent que l'asymétrie intrinsèque des liaisons hydrogène est responsable de l'orientation des molécules de surface. Et le modèle permet également de prédire la dépendance à la température de la tension superficielle de l'eau avec une précision de 1 %.
Cette étude démontre qu'il est possible d'appliquer le modèle de l'oscillateur de Drude à des domaines encore inexplorés. Elle offre ainsi, par exemple, des perspectives prometteuses pour l'exploration de la matièrematière condensée.