au sommaire

Les Led, qui ont elles-mêmes succédé aux ampoules à incandescence et aux lampes fluo-compactes, seront-elles bientôt remplacées par des cellules électrochimiques électroluminescentes (Lec) ? © Akimbomidget, CC, by-sa 2.5
D'une efficacité redoutable (jusqu'à 300 lumens par watt en laboratoire contre un maximum de 70 lm/W pour les lampes fluo-compactes et pas plus de 20 lm/W pour les lampes à incandescence de nos grands-parents) et d'une durée de vie exceptionnelle (jusqu'à 100.000 heures alors que les lampes fluo-compactes durent au maximum 15.000 heures et les lampes à incandescence pas plus de 1.000 heures), les Led apparaissent aujourd'hui comme des sources d’éclairage idéales. Selon l'AdemeAdeme, elles devraient s'imposer dans nos foyers dans moins de 5 ans.
Pourtant, les LedLed présentent également quelques défauts. Leur processus de fabrication, par exemple, est relativement énergivore. Car les Led sont des systèmes multicouches complexes dont les méthodes de production nécessitent un vide poussé et de hautes températures. Elles doivent également être protégées de toute exposition à l'air et à l'eau. De ce point de vue, les cellules électrochimiquescellules électrochimiques électroluminescentes (Lec) sont des dispositifs beaucoup plus simples. Elles ne comportent qu'une seule couche de matériaumatériau actif qui peut être travaillé en solution dans des conditions ambiantes et leurs électrodesélectrodes peuvent être réalisées à base de matériaux simples comme l'aluminium.
Si, malgré cela, les Lec n'ont pas jusqu'alors attiré l'attention sur elles, c'est que leur duréedurée de vie reste relativement courte. Un défaut que des chercheurs des universités de Bâle et de ValenceValence pourraient bien être sur le point de surmonter. Dans un article publié récemment dans le journal Chemical Science, ils annoncent avoir conçu des Lec à base de composés moléculaires stabilisés par des anneaux aromatiquesaromatiques dont la durée de vie sous forme de film mince est supérieure à 2.500 heures. « Ce n'est qu'un premier pas. Nous pouvons faire beaucoup mieux », assure Edwin Constable, professeur à l'université de Bâle.
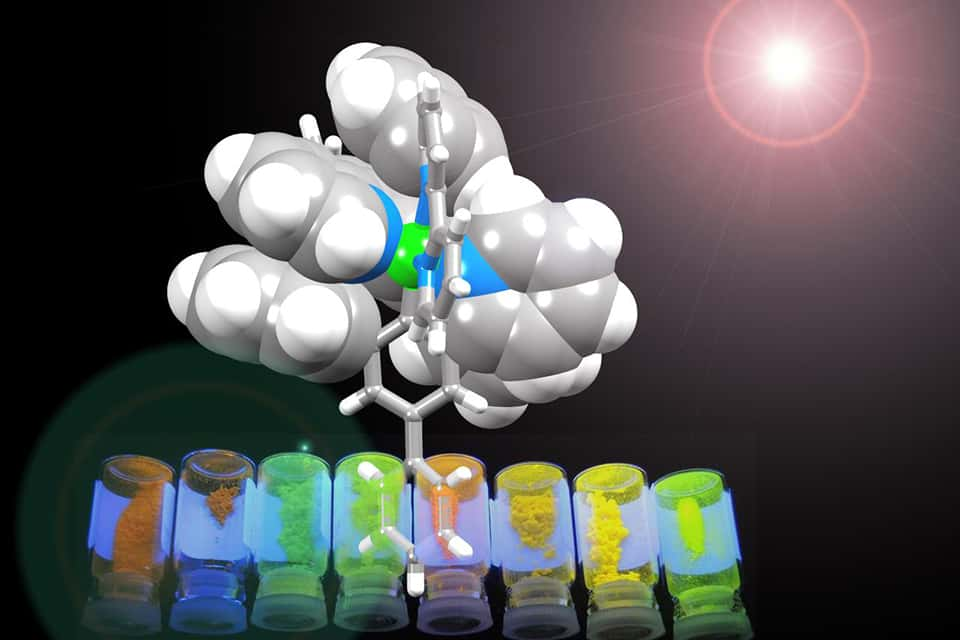
L’iridium, qui est ici au centre du dispositif Lec, est enveloppé d’une couche organique protectrice. La structure chimique précise de la couche organique permet de sélectionner la couleur de la lumière émise. © Université de Bâle
Des anneaux aromatiques inspirés des fleurs
Les métauxmétaux de transition, qui peuvent former des ionsions d'une grande variété, sont des matériaux de choix pour la constitution de la couche active de Lec. Après applicationapplication d'une polarisation, les charges présentes dans la couche active se déplacent vers les électrodes. Elles s'accumulent aux interfaces et provoquent ainsi une importante baisse de potentiel et la formation de zones fortement dopées. L'émissionémission de lumièrelumière a lieu dans la zone intrinsèque située entre les zones dopées.
Le ruthéniumruthénium, un métal de transitionmétal de transition de deuxième série est le premier des métaux de transition à avoir été utilisé pour la fabrication de Lec. Celles-ci n'étaient susceptibles d'émettre que dans le rouge ou l'orange. Elles étaient surtout très instables dans des conditions normalesconditions normales d'utilisation. Opter pour un métal de transition de troisième série comme l'iridiumiridium a permis aux chercheurs des universités de Bâle et de Valence d'améliorer la stabilité du système et de choisir la couleurcouleur d'émission lumineuse grâce à la formation de structures originales. Et l'équipe envisage déjà de remplacer l'iridium par des métaux d'usage courant et beaucoup plus abondants comme le cuivre.
Pour assurer une durée de vie élargie à leurs Lec, les chercheurs des universités de Bâle et de Valence ont donc mis au point des complexes métalliques enrichis d'anneaux aromatiques. Ceux-ci s'organisent entre eux pour former une coque protectrice, un peu comme une fleur dont les pétalespétales se referment sur son cœur pendant la nuit. Une structure qui rend le complexe particulièrement stable et qui permet également de choisir la couleur de la lumière émise selon les composants moléculaires sélectionnés. De quoi faire un pas de plus vers la conception de systèmes émetteurs de lumière blanche.






















