au sommaire

L'algue Closterium moniliferum prend une forme en croissant de lune. © Proyecto Agua/Water project, Flickr, CC by-nc-sa 2.0
- Tout savoir sur le traitement des déchets radioactifs

Avec l'actualité brûlante au Japon, l'énergie nucléaire est actuellement sur la sellette. Quelle que soit l'issue des débats qui s'ouvriront, le traitement des déchets radioactifs constitue déjà aujourd'hui un problème complexe, d'autant plus que d'autres activités (en dehors des centrales nucléaires) en produisent aussi, à l'image du monde médical où des isotopesisotopes radioactifs sont couramment utilisés.
Des solutions de traitement des déchets existent mais consistent majoritairement à les stocker profondément sous terre, dans des conteneurs que l'on espère étanches, une solution qui a remplacé le rejet en mer (abandonné il y a une vingtaine d'années). Parmi les déchets produits en grandes quantités suite aux fissions nucléairesfissions nucléaires, le strontiumstrontium 90 tient une belle place, au même titre que l'iode 131 ou le césium 137.
Strontium, calcium et barium : des métaux alcalino-ferreux
Le strontium 90 est particulièrement dangereux, sa demi-viedemi-vie étant de 28,8 ans. De plus, ses propriétés chimiques le rendent facilement assimilable par les organismes vivants. En effet, il possède les mêmes caractéristiques que le barium, mais surtout que le calciumcalcium, tous trois étant des métauxmétaux alcalino-ferreux (trois éléments consécutifs sur la deuxième colonne du tableau périodique des élémentstableau périodique des éléments). Ainsi, les organismes peuvent accumuler le strontium, bien qu'en faible quantité, dans les dents et les os, le confondant avec le calcium. Si cette erreur biologique est sans conséquence, l'incorporation de son isotope radioactif est beaucoup plus nocive, pouvant être à l'origine de cancerscancers.
Malheureusement, la quantité de calcium inoffensif produit par les réacteurs nucléaires est importante, et il est très difficile d'en isoler le strontium radioactif par des traitements classiques étant donné leurs réactivités chimiques similaires.
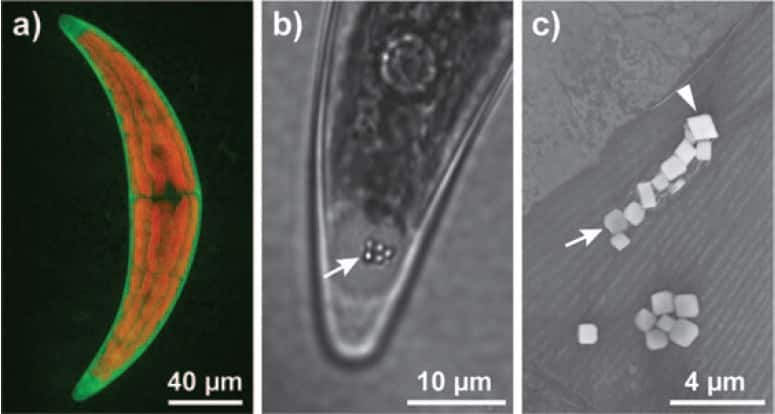
L'algue verte unicellulaire Closterium moniliferum (visible en entier en a) accumule des vésicules (flèche en b) formées de cristaux (flèche en c) à base de barium et de strontium. © ChemSusChem
Une algue verte pas comme les autres
L'algue verte unicellulaire Closterium moniliferum pourrait apporter la solution au problème. Cette algue en forme de croissant de lunelune est en effet particulière, car elle sait distinguer les trois éléments chimiqueséléments chimiques sans difficulté. Alors qu'elle utilise naturellement le barium trouvé dans l'eau pour construire des cristaux (de formule BaSO4) d'un micromètremicromètre de diamètre, qui formeront des vacuoles (dont le rôle est inconnu, mais pourrait être impliqué dans le stockage du sulfate) au niveau des deux extrémités de la cellule, elle le confond parfois avec le strontium... mais presque jamais avec le calcium !
On savait qu'elle était ainsi capable de former des cristaux mixtes, contenant du barium et du strontium (de formule (Ba,Sr)SO4), le barium étant d'ailleurs indispensable à l'initiation de la formation d'un cristal (il n'y a pas de formation de cristaux s'il n'y a que du strontium dans le milieu), mais l'on n'en connaissait pas les proportions.
Une efficacité qui reste à prouver
Dans une nouvelle étude parue dans la revue ChemSusChem, les chercheurs du Northwestern University à Evanston aux États-Unis ont montré que les algues peuvent fabriquer des cristaux formés en grande partie de strontium (20 à 45 %), dès lors qu'elles sont placées dans un milieu enrichi en strontium et appauvri en barium. En revanche, cette même expérience menée avec du calcium à la place du strontium ne permet que l'incorporation de 5 % de calcium dans les cristaux.
Ces résultats font de Closterium moniliferum un bon candidat pour le traitement des déchets radioactifsdéchets radioactifs à base de strontium 90. En effet, les cristaux sont rapidement obtenus (en 30 à 40 minutes) et sont stables, même si l'on place ensuite les algues dans un milieu privé des deux éléments. Maintenant, de nouvelles études doivent prouver que la présence des mêmes éléments radioactifs n'empêchera pas l'algue d'accomplir sa mission...