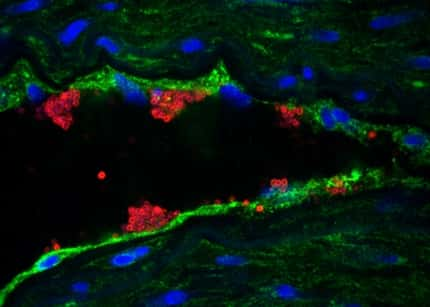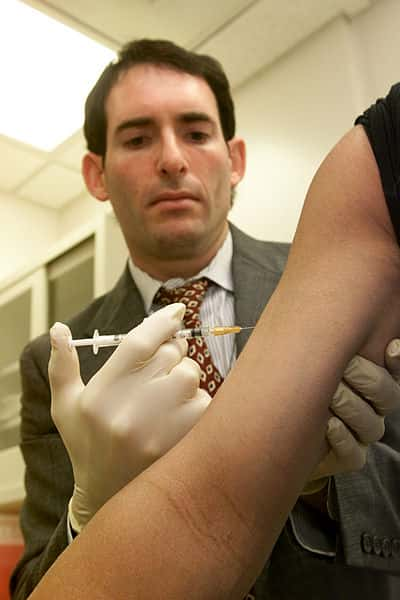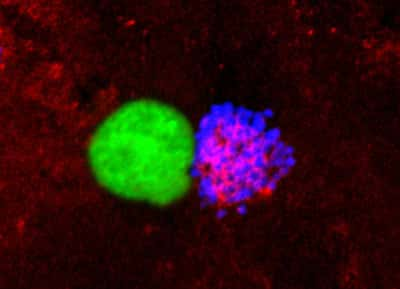
L'infection des cellules endothéliales de la paroi des vaisseaux par le méningocoque (en bleu) entraîne un recrutement massif des protéines d'adhérence (en rouge), ce qui empêche leur accumulation au point de contact des globules blancs (ou leucocytes) (e
Cette équipe vient de démontrer l'étonnante capacité des bactéries à retarder la traversée de la paroi vasculaire par les globules blancs. Il pourrait s'agir là d'un mécanisme mis en œuvre par le méningocoque pour se préserver momentanément de la réponse anti-infectieuse, ce qui expliquerait en partie sa virulence.
Le méningocoque, germegerme responsable de méningites et de septicémies chez l'homme, est une bactérie assez répandue dans la population puisque 10 à 15% des individus sont des porteurs sains (sans symptômesymptôme), le germe colonisant alors le nasopharynx.
Les méningites à méningocoquesméningites à méningocoques sont rares en France où l'incidenceincidence de ces infections se situe autour de 1 cas pour 100 000 habitants, mais sa gravitégravité réside dans son pronosticpronostic fatal (10% des cas). En effet, on dénombre chaque année dans notre pays une trentaine de décès par infection méningococcique et la létalité de cette affection semble en augmentation depuis plusieurs années. Ces infections touchent surtout les enfants de moins de 5 ans (avec un pic de fréquence à l'âge de 4 mois), et les adolescents. De plus ces méningites prennent parfois une forme épidémique affectant alors des milliers de personnes en Afrique. Les vaccinsvaccins actuels contre les sérogroupes A et C sont peu efficaces pour la protection des jeunes enfants et aucun vaccin n'est actuellement disponible contre le sérogroupe B, à l'origine de petites épidémiesépidémies et de cas sporadiques de plus en plus nombreux en Europe.
Du fait de la sélectivité de N. meningitidis pour l'homme, aucun modèle animal de l'infection n'a pu être développé et très peu de données ont pu être obtenues sur les mécanismes d'interaction in situ de cette bactérie avec son hôte. La contribution majeure du partenariat entre l'équipe de Sandrine Bourdoulous (Institut Cochin) et de Xavier Nassif (Faculté de Médecine Necker - Enfants Malades) a été d'élucider les mécanismes du passage des bactéries à travers la barrière hémato-encéphaliquebarrière hémato-encéphalique. Pour ce faire, les méningocoques détournent la machinerie des cellules qu'ils infectent et induisent au niveau de ces dernières des projections qui les englobent. Ces équipes ont également montré que les méningocoques facilitent leur entrée dans les cellules en utilisant un récepteur de la famille du récepteur du facteur de croissancefacteur de croissance EGF. Ce récepteur impliqué dans la différenciation et la prolifération cellulaires, stimule aussi la progression de nombreuses tumeurstumeurs du sein et de l'ovaireovaire.
Dans leurs travaux publiés le 22 mai dans la revue J Cell Biol, les équipes de l'Institut Cochin et de l'Institut Necker - Enfants Malades montrent à présent un nouveau mécanisme par lequel les méningocoques peuvent retarder l'initiation d'une réponse inflammatoire. Celle-ci débute par un recrutement des globules blancs (ou leucocytes) au site infecté. Or, la machinerie cellulaire responsable du franchissement des vaisseaux sanguins par les globules blancs et par les méningocoques est similaire, si bien qu'elle est engagée dans son interaction avec les bactéries et indisponible pour le passage des globules blancs. Il s'ensuit sans doute un retard dans l'intervention anti-infectieuse des leucocytes à l'intérieur du liquide céphalorachidienliquide céphalorachidien, ce qui pourrait en diminuer l'efficacité. Ces résultats permettent de mieux comprendre les interactions entre les méningocoques et les globules blancs dans le franchissement de la barrière entre le sang et le liquide céphalorachidien, et donc de préciser certains mécanismes fondamentaux de la virulence de ce redoutable agent infectieux. De telles données sont précieuses pour tenter d'améliorer les stratégies thérapeutiques.
Notes :
1) UMR 8104/CNRS, InsermU567, UM3 de l'Université René DescartesRené Descartes
2) INSERM U570, Faculté de Médecine Necker-Enfants Malade
Références :
1) Hoffmann I, Eugene E, Nassif X, Couraud PO et Bourdoulous S. "Activation of ErbB2 tyrosinetyrosine kinasekinase receptor supports invasion of endothelial cells by Neisseria meningitidis" J. Cell Biol (2001) 155:133-143.
2) Doulet N, Donnadieu E, Laran-Chich MP, Niedergang F, Nassif X, Couraud PO et Bourdoulous S "Neisseria meningitidis infection of human endothelial cells interferes with leukocyte transmigration by preventing the formation of endothelial docking structures" J. Cell Biol (2006) 173:627-637.
Contacts :
Chercheurs :
Institut Cochin
Sandrine Bourdoulous (CNRS)
Tél. : 01 40 51 64 27
bourdoulous@cochin.inserm.fr
Faculté de médecine Necker - Enfants Malades
Xavier Nassif (Inserm)
Tél. : 01 40 61 56 78
nassif@necker.fr
Presse CNRS :
Muriel Ilous
Tél. : 01 44 96 43 09
muriel.ilous@cnrs-dir.fr
Institut Cochin :
Claude Charfi
Tél. : 01 40 51 64 57
charfi@cochin.inserm.fr