au sommaire
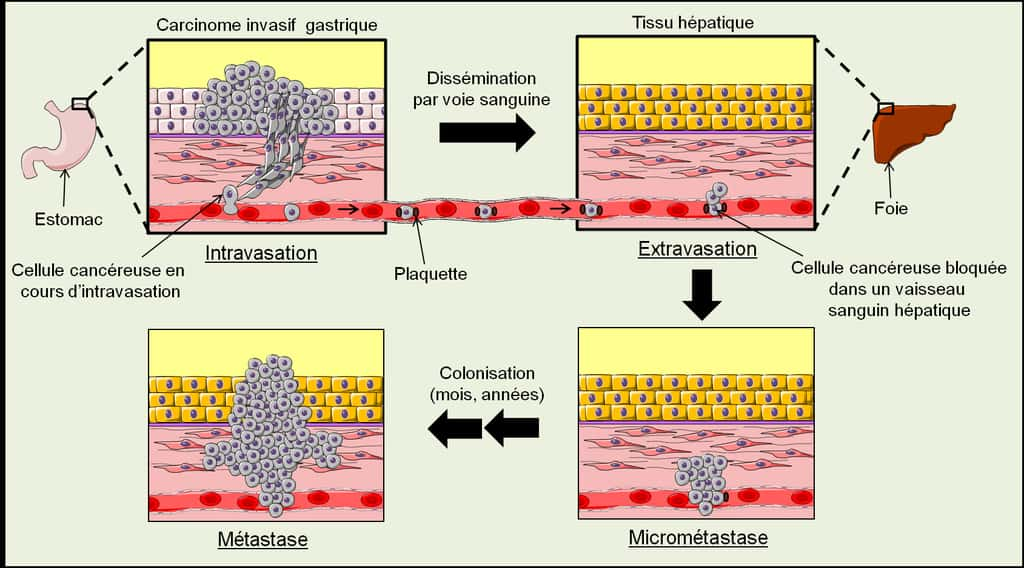
Les gènesgènes suppresseurs de tumeurssuppresseurs de tumeurs sont des garde-fousgarde-fous qui empêchent la dérive d'une cellule vers la malignité. C'est la raison pour laquelle de nombreux gènes suppresseurs de tumeurs sont inactivés dans les cancerscancers.
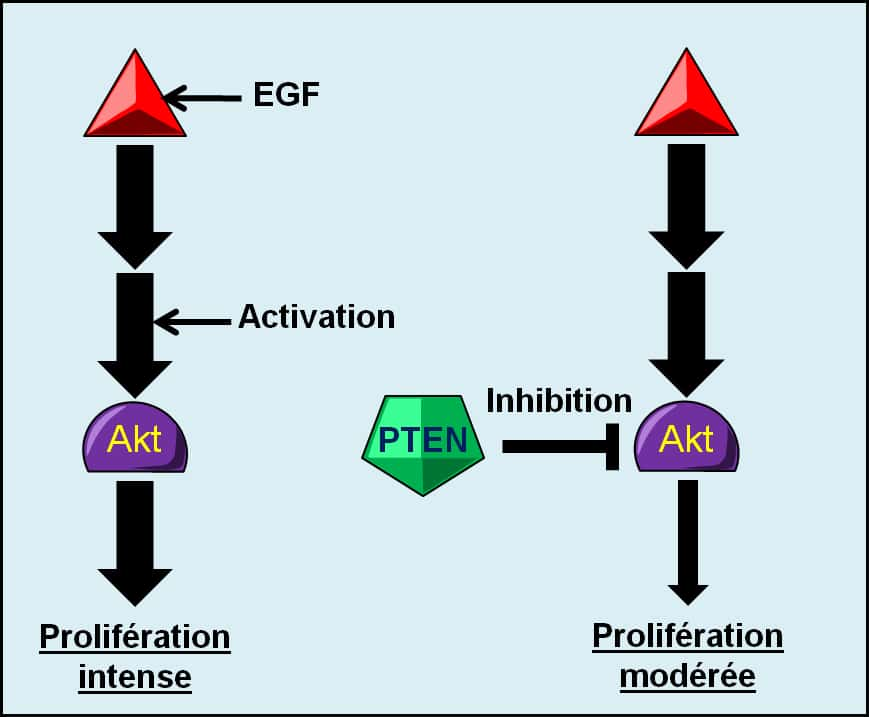
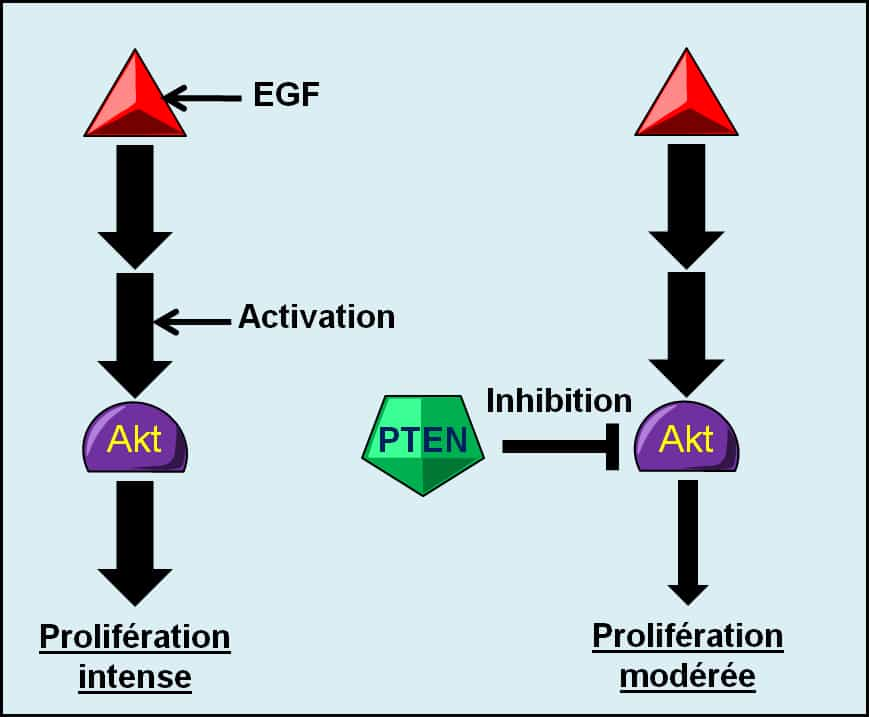
Figure 11. Mode d’action schématique du gène suppresseur de tumeurs PTEN. En l’absence de contrôle par PTEN, Akt active intensément la prolifération cellulaire lorsqu’elle est stimulée par l’EGF. Si PTEN exerce son contrôle sur Akt, la prolifération cellulaire est modérée. © Grégory Ségala
Les gènes suppresseurs de tumeurs agissent soit en inhibant des mécanismes qui favorisent l'oncogenèseoncogenèse, soit en activant des mécanismes qui empêchent l'oncogenèse. Les gènes suppresseurs de tumeurs sont inactivés au cours de l'oncogenèse.
Les gènes suppresseurs de tumeurs régulateurs de la prolifération
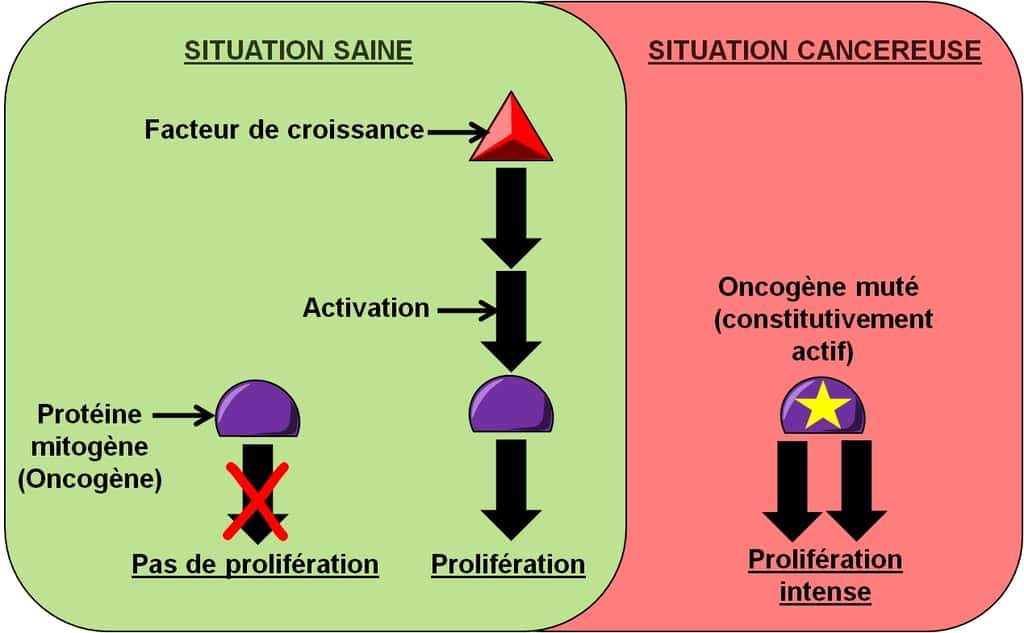
Au cours du cycle cellulaire, le gène suppresseur de tumeur Rb est la dernière barrière s'opposant à une prolifération incontrôlée mais d'autres barrières existent en amont de Rb, dans les voies mitogènes. Ces voies de signalisation sont composées de nombreuses protéinesprotéines-relais qui transmettent le signal entre l'émetteur (le facteur de croissancefacteur de croissance) et le récepteur final de ce signal (la protéine Rb). Des gènes suppresseurs de tumeurs contrôlent certains de ces relais de signalisation en les inhibant, ce qui a pour conséquence d'inhiber la voie de signalisation de la prolifération.
Parmi ces gènes, on compte par exemple le gène suppresseur de tumeurs PTEN qui inhibe l'oncogèneoncogène Akt dans la voie de signalisation de l'EGF (Figure 11). Ce contrôle permet de modérer les signaux de prolifération pour éviter une prolifération cellulaire trop intense ou cela permet de remettre la voie de signalisation au repos en l'absence de facteur de croissance. De cette façon, l'intensité des signaux de prolifération est contrôlée et la prolifération cellulaire reste dépendante d'une stimulationstimulation extérieure par un facteur de croissance, elle n'est pas autonome. Les cellules cancéreuses inactivent donc des gènes suppresseurs de tumeurs contrôlant les voies de signalisation de la prolifération cellulaire pour bénéficier d'une prolifération intense et autonome.
Les mécanismes de maintenance du génome
Dans une cellule, il existe des mécanismes qui surveillent l'intégritéintégrité du génomegénome pour empêcher l'apparition de cellules mutées qui peuvent dériver vers un cancer.
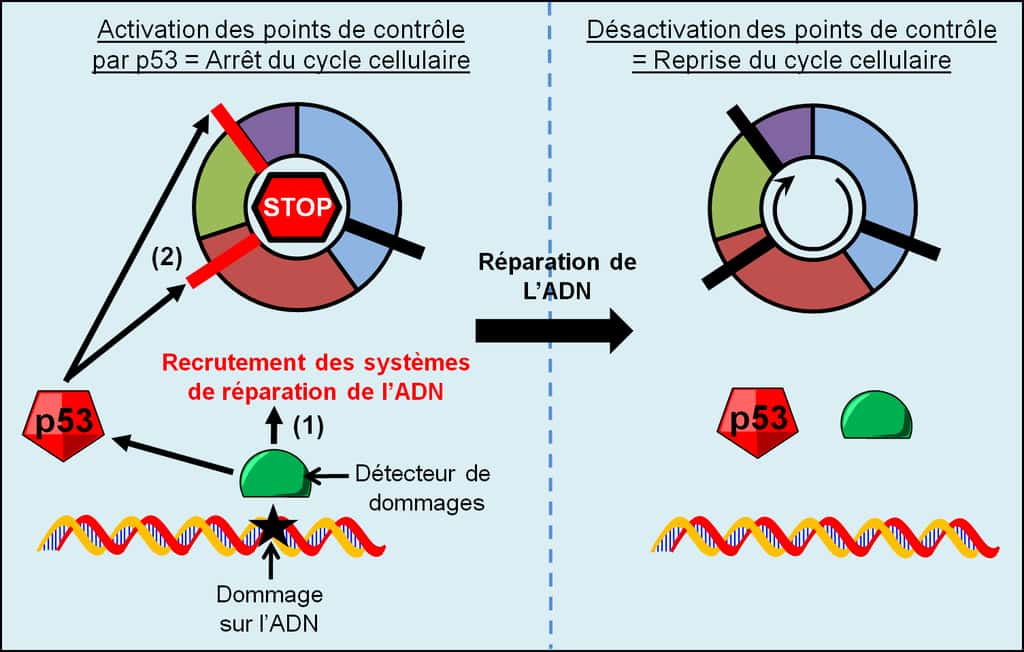
Figure 12. Signalisation et réparation des dommages de l’ADN. Lors de dommages sur l’ADN, les détecteurs de dommages de l’ADN activent les systèmes de réparation de l’ADN ainsi que p53 qui arrête le cycle cellulaire. Après la réparation de l’ADN, la signalisation des dommages de l’ADN n’est plus active et le cycle cellulaire reprend. © Grégory Ségala
Lorsque des dommages surviennent sur l'ADNADN, comme des mutations ou des cassures, les mécanismes de signalisation des dommages de l'ADN avertissent de ces dégâts pour qu'ils soient corrigés par les systèmes de réparation de l'ADN (Figure 12, (1)). Le gène suppresseur de tumeurs p53p53 occupe une position centrale dans la signalisation des dommages de l'ADN, ce qui lui vaut le surnom de « gardien du génome ». Si ces dommages peuvent être réparés et qu'un cycle cellulaire est engagé, p53 active les points de contrôle du cycle cellulaire (Figure 12,(2)) ce qui provoque l'arrêt du cycle cellulaire jusqu'à ce que les mutations ou cassures de l'ADN soient réparés.
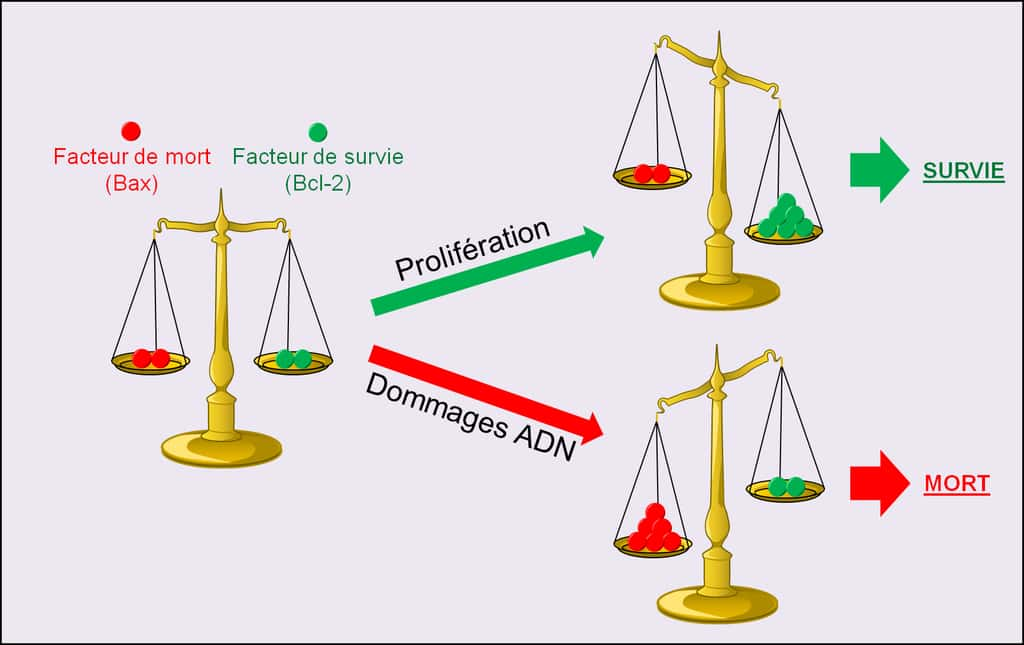
Si les dommages de l'ADN sont graves, p53 provoque la mort programmée de la cellule par apoptoseapoptose qui est un mécanisme sophistiqué de suicide de la cellule (Figure 13).
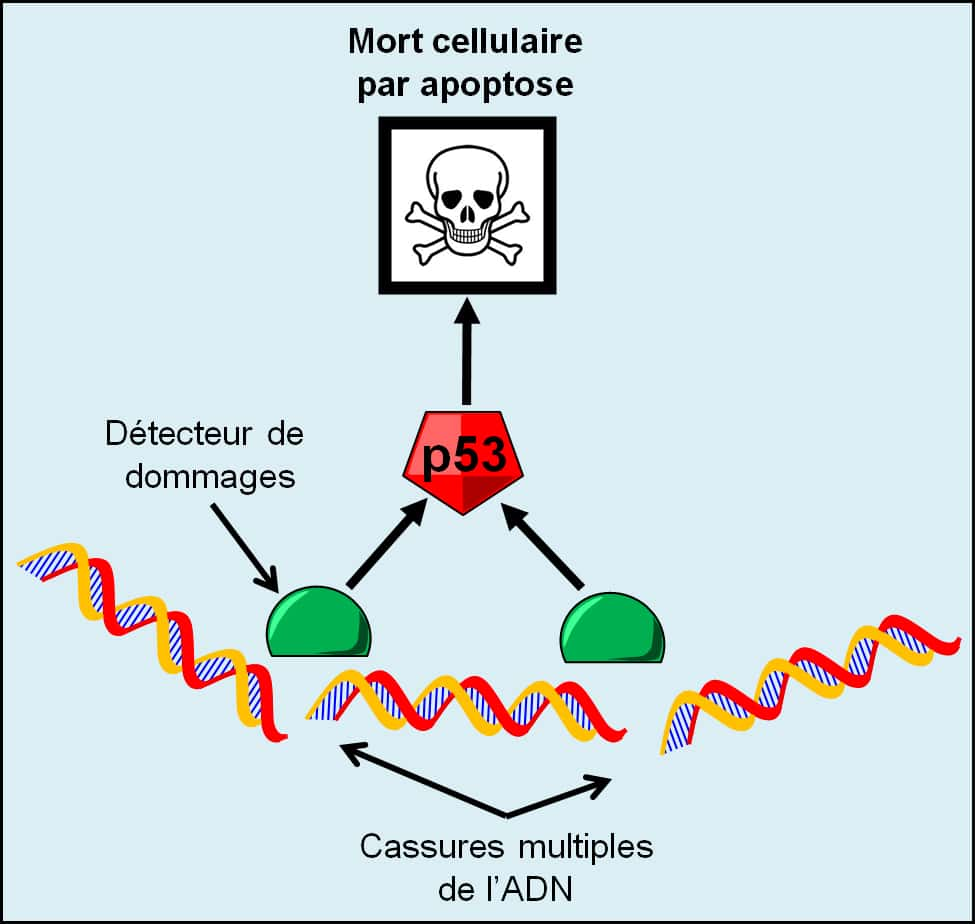
Figure 13. Signalisation de dommages importants de l’ADN. Après que l’ADN a subi d’importants dommages comme des cassures multiples, la signalisation des dommages de l’ADN provoque la mort de la cellule par apoptose. © Grégory Ségala
Dans les cancers, on relève un dysfonctionnement de la signalisation des dommages à l'ADN puisque la conservation de mutations de l'ADN favorise la progression de l'oncogenèse. D'autre part, ce dysfonctionnement diminue la fréquence d'activation des points de contrôle du cycle cellulaire. Le cycle cellulaire est donc moins stoppé ce qui permet aux cellules cancéreuses de proliférer plus rapidement. Enfin, comme nous allons le voir dans le chapitre suivant, l'instabilité génétiquegénétique est forte dans les cellules cancéreuses ce qui se traduit par d'importants dommages sur l'ADN. Normalement ces dommages provoqueraient la mort de la cellule. C'est pourquoi un défaut de signalisation des dommages de l'ADN permet aussi à la cellule cancéreuse de survivre à des dommages plus importants.